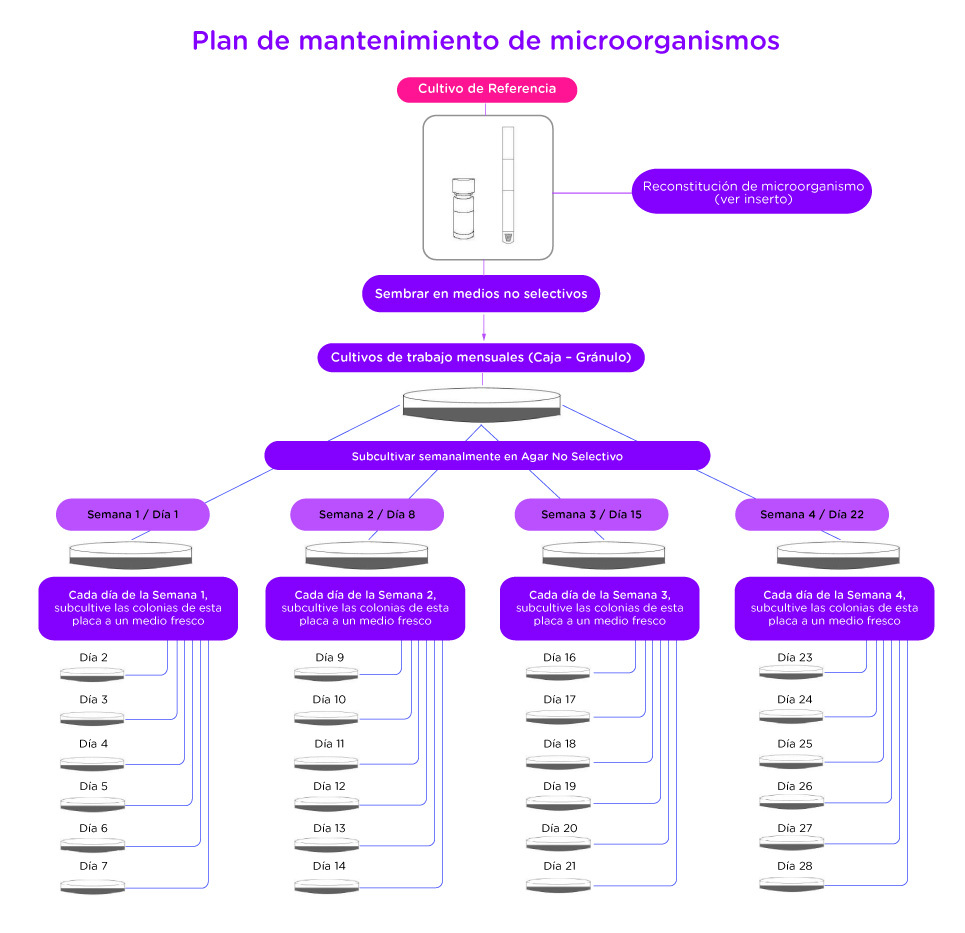
El mantenimiento adecuado de las cepas de control de calidad es esencial para asegurar el desempeño adecuado de cualquier tipo de laboratorio. Esta publicación consiste en un plan de mantenimiento para preservar la viabilidad, pureza, y características genotípicas y fenotípicas de una cepa. La mayoría de las cepas de MicroBioLogics se pueden mantener por más de un mes, después de su reconstitución.
Primer paso:
Los microorganismos de MicroBioLogics se deben resucitar en un medio no selectivo, como Agar Tripticasa de Soya o Agar Sangre. Sin embargo, hay requerimientos especiales para ciertos tipos de microorganismos. No se recomienda hacer este paso en caldos, ya que estos se contaminan fácilmente.
Almacenamiento de Microorganismos Reconstituidos:
- La mayoría de microorganismos se pueden mantener en placas de medios no selectivos o tubos inclinados, hasta por cuatro semanas; ya sea a temperatura ambiente o en refrigeración.
- Los microorganismos exigentes tienen periodos de vida más cortos que las bacterias aeróbicas. Estos deberán ser subcultivados a los pocos días. Ejemplos: Streptococcus pneumoniae y Neisseria gonorrhoeae se deben repicar cada tres días.
- MicroBioLogics sugiere las siguientes condiciones de almacenamiento para favorecer el mantenimiento de las cepas:
| Categoría de Microorganismo | Condiciones de Almacenamiento |
| Bacterias Aeróbicas | Almacenar a 2-8°C. Algunas especies de Bacillus se mantienen viables por largos periodos almacenadas a temperatura ambiente. |
| Especies dependientes de CO2 | Almacenar a temperatura ambiente en un contenedor con un sobre de CO2. |
| Mohos y Levaduras | Almacenar a temperatura ambiente. |
| Anaerobios | Almacenar en condiciones anaeróbicas y a temperatura ambiente. |
| Campylobacter | Almacenar en Agar Chocolate a 35°C en condiciones de microaerofilia. |
- Los microorganismos almacenados a 4°C no se pueden usar en algunas pruebas.
- Si el cultivo resucitado es congelado, MicroBioLogics no puede garantizar que se mantengan las características del producto.
Consejos para un mejor desempeño
- No utilice la caja que contiene la siembra del gránulo original para evaluar las características fenotípicas. Aquí el microorganismo no se encuentra totalmente desarrollado.
- Seleccione colonias aisladas para las pruebas. No use colonias a partir de placas contaminadas.
- Utilice cultivos frescos, con no más de 24 horas para hacer pruebas bioquímicas.
- Puede ser necesario utilizar nuevos microorganismos para las pruebas de susceptibilidad a antibióticos, cada dos semanas, ya que algunas cepas van perdiendo resistencia a través del tiempo.
- Algunos ensayos farmacopeicos, como las pruebas de promoción de crecimiento, no aceptan cultivos con más de cinco pases a partir del cultivo de referencia.
Para terminar:
- Después de la cuarta semana, descarte las placas de cultivos y empiece una vez más el proceso con un nuevo gránulo liofilizado.
- Un microorganismo puede ser utilizado después de la fecha de vencimiento si: (1) el gránulo liofilizado fue reconstituido antes de su fecha de vencimiento, y (2) el microorganismo no se usa después de la cuarta semana del programa de mantenimiento.
REFERENCIAS
1. CLSI M07-A10, Vol. 35 No. 2, Methods for Dilution Antimicrobial Susceptibility Tests for Bacteria that Grow Aerobically: Approved Standard – Tenth Edition, Clinical Standards Laboratory Institute. Abril 2015.
2. Boletín Técnico Informativo de Requerimientos de Crecimiento: www.microbiologics.com, Support Center/Document Library/Technical Information Bulletins
3. Farmacopea de los Estados Unidos 38 NF 33, <61> Microbiological Examination of Nonsterile Products: Microbial Enumeration Tests. 2015
4. ISO 11133, Microbiology of food, animal feed and water – Preparation, production, storage and performance testing of culture media. Primera edición 2014-05-15.